컴퓨터 보조 검출
컴퓨터 보조 검출 (CADe)은 컴퓨터 보조 진단 (CADx)이라고도 하며, 의사가 의료 영상을 해석하는 것을 지원하는 시스템이다. X선, MRI, 내시경, 초음파 진단 등의 영상 기술은 방사선 전문의나 기타 의료 전문가가 짧은 시간 내에 종합적으로 분석하고 평가해야 하는 방대한 양의 정보를 생성한다. CAD 시스템은 디지털 영상이나 동영상을 처리하여 전형적인 소견을 찾아내고, 질병 가능성이 있는 부분과 같은 주목할 만한 영역을 강조 표시하여 전문가의 의사결정을 지원하는 정보를 제공한다.
CAD는 전체 슬라이드 영상화 및 기계 학습 알고리즘의 등장과 함께 디지털 병리학 분야에서도 잠재적인 미래 응용 가능성을 가지고 있다. 지금까지 그 적용은 면역염색의 정량화에 한정되어 왔으나, 표준 H&E 염색에 대한 연구도 진행 중이다.[^12]
CAD는 인공지능과 컴퓨터 비전의 요소를 방사선학 및 병리학 영상 처리와 결합한 학제간 기술이다. 대표적인 응용 사례는 종양의 검출이다. 예를 들어, 일부 병원에서는 유방 촬영술(유방암 진단), 대장 내시경에서의 용종 검출, 폐암 검출 등의 예방적 건강검진을 지원하기 위해 CAD를 사용한다.
컴퓨터 보조 검출(CADe) 시스템은 일반적으로 주목할 만한 구조와 영역을 표시하는 데 한정된다. 컴퓨터 보조 진단(CADx) 시스템은 주목할 만한 구조를 평가한다. 예를 들어, 유방 촬영술에서 CAD는 미세석회화 군집과 연조직 내의 고밀도 구조를 강조 표시한다. 이를 통해 방사선 전문의는 병리 상태에 대한 결론을 도출할 수 있다. 또 다른 응용 분야는 CADq로, 종양의 크기나 조영제 흡수에서의 종양 거동 등을 정량화한다. 컴퓨터 보조 간이 분류(CAST)는 또 다른 유형의 CAD로, 완전 자동으로 초기 해석을 수행하고 검사를 의미 있는 범주(예: 음성 및 양성)로 분류한다. CAST는 생명을 위협하는 중대한 상태에 대한 신속한 진단이 요구되는 응급 진단 영상에서 특히 유용하다.
CAD는 40년 이상 임상 환경에서 사용되어 왔지만, 일반적으로 의사나 기타 전문가를 대체하지 않으며 오히려 보조적 역할을 수행한다. 전문가(일반적으로 방사선 전문의)가 의료 영상의 최종 해석에 대한 책임을 진다.[^13] 그러나 일부 CAD 시스템의 목표는 당뇨망막병증, 유방 촬영술에서의 구조적 왜곡,[^14][^15] 흉부 CT에서의 간유리 결절,[^16][^17] CT 대장조영술에서의 비용종성("평탄") 병변[^18] 등과 같이 인간 전문가가 발견할 수 없는 환자의 가장 초기 이상 징후를 검출하는 것이다.
역사
1950년대 후반, 현대 컴퓨터의 여명과 함께 다양한 분야의 연구자들은 컴퓨터 보조 의료 진단(CAD) 시스템을 구축할 가능성을 탐색하기 시작했다.[^19] 이러한 초기 CAD 시스템들은 순서도, 통계적 패턴 매칭, 확률 이론 또는 지식 기반을 사용하여 의사결정 과정을 수행했다.[^1]
1970년대 초, 의학 분야에서 흔히 "전문가 시스템"이라고 불리던 매우 초기의 CAD 시스템들이 개발되어 주로 교육 목적으로 사용되었다. 그 예로는 MYCIN 전문가 시스템,[^20] Internist-I 전문가 시스템,[^21] CADUCEUS 전문가 시스템이 있다.[^22] 진단 로봇은 자동 진단 시스템으로서 지식 기반 하위 시스템을 통해 의료 진단을 위한 데이터를 수집할 수 있으며, 건 구동식 인간형 손가락, 촉각 인지를 위한 피부형 센서와 같은 도구들이 구상되었다.[^2][^3]
연구자들은 처음에 컴퓨터의 능력에 대한 비현실적인 낙관론을 가지고 완전히 자동화된 CAD / 전문가 시스템을 구축하는 것을 목표로 했다. 그러나 리처드 M. 카프의 획기적인 논문 "조합 문제들 간의 환원 가능성"[^23] 이후, 중요한 계산 문제 그룹을 해결하기 위한 알고리즘 개발에는 잠재적 가능성뿐만 아니라 한계도 있다는 것이 명확해졌다.[^1] 1970년대 초 카프가 발견한 다양한 알고리즘적 한계에 대한 새로운 이해에 대응하여, 연구자들은 의학 분야에서 CAD 및 전문가 시스템의 심각한 한계를 인식하기 시작했으며,[^1] 이는 그들이 고급 접근 방식을 사용하여 새로운 종류의 CAD 시스템을 개발하도록 이끌었다. 이에 따라 1980년대 후반과 1990년대 초에는 보다 진보되고 유연한 CAD 시스템을 구축하기 위한 데이터 마이닝 접근법의 활용으로 초점이 전환되었다. 1998년, 유방 촬영술을 위한 최초의 상용 CAD 시스템인 ImageChecker 시스템이 미국 식품의약국(FDA)의 승인을 받았다. 이후 수년간 유방 촬영술, 유방 MRI, 폐·대장·심장의 의료 영상을 분석하는 여러 상용 CAD 시스템도 FDA 승인을 받았다. CAD 시스템은 의사를 위한 진단적 의료 의사결정 보조 도구로 사용되기 시작했다.[^24]
2013년 2월, IBM은 왓슨 소프트웨어 시스템의 최초 상용 응용이 웰포인트(현 앤섬)와 협력하여 메모리얼 슬론 케터링 암센터에서 폐암 치료의 이용 관리 결정에 활용될 것이라고 발표했다. 2013년, IBM 왓슨의 사업 책임자 마노지 삭세나는 왓슨을 사용한 현장 간호사의 90%가 왓슨의 지침을 따랐다고 밝혔다.^25
방법론
CAD는 근본적으로 매우 복잡한 패턴 인식에 기반한다. X선 또는 다른 유형의 영상에서 의심스러운 구조를 탐색한다. 일반적으로 알고리즘을 최적화하기 위해 수천 장의 영상이 필요하다. 디지털 영상 데이터는 DICOM 형식으로 CAD 서버에 복사되며, 여러 단계를 거쳐 준비 및 분석된다.
1. 전처리 목적:
- 아티팩트(영상 결함) 감소
- 영상 노이즈 감소
- 다양한 기본 조건(예: 서로 다른 노출 매개변수)에 따른 영상 품질의 평준화(조화) 및 대비 향상
- 필터링
2. 분할 목적:
- 영상 내 다양한 구조의 구별, 예: 심장, 폐, 흉곽, 혈관, 원형 병변 가능성
- 해부학적 데이터뱅크와의 대조
- 관심 영역 내 표본 회색값 분석[^27]
3. 구조/ROI(관심 영역) 분석 검출된 각 영역은 다음과 같은 특수 특성에 대해 개별적으로 분석된다:
- 밀집도
- 형태, 크기 및 위치
- 인접 구조/ROI와의 관계
- ROI 내 평균 회색값 분석
- ROI 내부 구조의 경계에 대한 회색값 비율
4. 평가/분류 구조 분석이 완료된 후, 각 ROI는 진양성(TP) 확률에 대해 개별적으로 평가(점수화)된다. 다음 절차들은 분류 알고리즘의 예시이다.
- 최근접 이웃 규칙 (예: k-최근접 이웃)[^28]
- 최소 거리 분류기
- 캐스케이드 분류기
- 나이브 베이즈 분류기
- 인공 신경망[^29][^30][^31][^32][^33]
- 방사 기저 함수 네트워크 (RBF)
- 서포트 벡터 머신 (SVM)[^34][^35]
- 주성분 분석 (PCA)
검출된 구조가 특정 임계값 수준에 도달하면, 영상의학과 전문의를 위해 영상에 강조 표시된다. CAD 시스템에 따라 이러한 표시는 영구적 또는 임시적으로 저장될 수 있다. 후자의 장점은 영상의학과 전문의가 승인한 표시만 저장된다는 것이다. 오탐은 저장하지 않는 것이 바람직한데, 이후 검사 시 판독이 더 어려워지기 때문이다.
제공자 지표와의 관계
민감도와 특이도
CAD 시스템은 의심스러운 구조를 강조하는 것을 목표로 한다. 오늘날의 CAD 시스템은 병리학적 변화의 100%를 검출할 수 없다. 검출률(민감도)은 시스템과 적용 분야에 따라 최대 90%에 이를 수 있다.[^36] 정확한 검출을 진양성(TP)이라 하며, 건강한 부위의 잘못된 표시는 위양성(FP)을 구성한다. FP가 적게 표시될수록 특이도가 높아진다. 낮은 특이도는 사용자가 이러한 모든 오탐을 식별해야 하므로 CAD 시스템의 수용성을 저하시킨다. 폐 개요 검사(CAD 흉부)에서 FP율은 검사당 2건으로 줄일 수 있었다. 다른 분야(예: CT 폐 검사)에서는 FP율이 25건 이상이 될 수 있다. CAST 시스템에서는 의미 있는 검사 분류를 가능하게 하기 위해 FP율이 극도로 낮아야 한다(검사당 1건 미만).
절대 검출률
영상의학과 전문의의 절대 검출률은 민감도와 특이도에 대한 대안적 지표이다. 전반적으로, 민감도, 특이도 및 절대 검출률에 관한 임상 시험 결과는 상당히 다를 수 있다. 각 연구 결과는 그 기본 조건에 따라 달라지며 해당 조건에 근거하여 평가되어야 한다. 다음 요인들이 강한 영향을 미친다:
- 후향적 또는 전향적 설계
- 사용된 영상의 품질
- X선 검사의 조건
- 영상의학과 전문의의 경험 및 교육 수준
- 병변의 유형
- 고려 대상 병변의 크기
과제
컴퓨터의 등장 이래 CAD가 이룩한 수많은 발전에도 불구하고, 오늘날 CAD 시스템이 직면하고 있는 특정 과제들이 여전히 존재한다.[^4]
일부 과제는 입력 데이터 수집, 전처리, 처리 및 시스템 평가를 포함하는 CAD 시스템의 절차에서 다양한 알고리즘적 한계와 관련이 있다. 알고리즘은 일반적으로 하나의 가능성 있는 진단을 선택하도록 설계되어 있어, 여러 질환이 동시에 존재하는 환자에게는 최적이 아닌 결과를 제공한다.[^37] 오늘날 CAD의 입력 데이터는 대부분 전자건강기록(EHR)에서 수집된다. EHR의 효과적인 설계, 구현 및 분석은 모든 CAD 시스템에서 매우 중요한 필수 요소이다.[^4]
대규모 데이터의 가용성과 이러한 데이터를 분석해야 하는 필요성으로 인해, 빅데이터 역시 오늘날 CAD 시스템이 직면한 가장 큰 과제 중 하나이다. 점점 방대해지는 환자 데이터는 심각한 문제이다. 환자 데이터는 종종 복잡하며 반정형 또는 비정형 데이터일 수 있다. 이를 합리적인 시간 내에 저장, 검색 및 분석하기 위해서는 고도로 발전된 접근 방식이 필요하다.[^4]
전처리 단계에서 입력 데이터는 정규화되어야 한다. 입력 데이터의 정규화에는 노이즈 감소와 필터링이 포함된다.
처리 과정은 응용 분야에 따라 몇 가지 하위 단계를 포함할 수 있다. 의료 영상에서의 기본적인 세 가지 하위 단계는 분할, 특징 추출/선택, 그리고 분류이다. 이러한 하위 단계들은 적은 연산 시간으로 입력 데이터를 분석하기 위한 고급 기법을 필요로 한다. CAD 시스템의 이러한 절차들을 위한 혁신적인 기법 개발에 많은 노력이 투입되었음에도, 각 개별 단계에서 단일 최적 알고리즘은 아직 등장하지 않았다. CAD 시스템의 모든 측면에서 혁신적인 알고리즘을 구축하기 위한 지속적인 연구가 필수적이다.[^4]
CAD 시스템에 대한 표준화된 평가 기준의 부재 또한 문제이다.[^4] 이러한 사실은 FDA와 같은 규제 기관으로부터 상용화 승인을 얻는 데 어려움을 초래할 수 있다. 또한 CAD 시스템의 많은 긍정적 발전이 입증되었음에도, 임상 실무에서의 알고리즘 검증을 위한 연구는 아직 확인되지 않았다.[^38]
그 밖의 과제들은 의료 제공자들이 임상 실무에서 새로운 CAD 시스템을 도입하는 문제와 관련이 있다. 일부 부정적인 연구 결과가 CAD의 사용을 저해할 수 있다. 또한 의료 전문가들이 CAD 사용에 대한 교육이 부족한 경우, 시스템 결과를 잘못 해석하는 경우가 발생하기도 한다.
응용 분야
![Medical Sieve의 인터페이스, 임상 결정을 지원하기 위한 [IBM 의 알고리즘]] CAD는 유방암, 폐암, 대장암, 전립선암, 골전이, 관상동맥 질환, 선천성 심장 결함, 병리학적 뇌 검출, 골절 검출, 알츠하이머병, 당뇨병성 망막병증의 진단에 사용된다.
유방암
CAD는 선별 유방촬영술(여성 유방의 X선 검사)에 사용된다. 선별 유방촬영술은 유방암의 조기 발견에 사용된다. CAD 시스템은 종양을 악성(암성) 또는 양성(비암성)으로 분류하는 데 자주 활용된다. CAD는 특히 미국과 네덜란드에서 확립되어 있으며, 일반적으로 영상의학과 전문의에 의한 인간 평가에 추가적으로 사용된다.
최초의 유방촬영술용 CAD 시스템은 시카고 대학교의 연구 프로젝트에서 개발되었다. 현재 iCAD와 Hologic에서 상업적으로 제공되고 있다. 그러나 높은 민감도를 달성하면서도, CAD 시스템은 매우 낮은 특이도를 보이는 경향이 있으며 CAD 사용의 이점은 여전히 불확실하다. 2008년의 선별 유방촬영술에서의 컴퓨터 보조 검출에 관한 체계적 문헌 고찰에서는 CAD가 암 검출률에 유의미한 영향을 미치지 않지만, 바람직하지 않게 재검률(즉, 위양성률)을 증가시킨다고 결론지었다. 그러나 연구 간 재검률에 대한 영향에서 상당한 이질성이 있음을 지적했다.[^39]
최근 기계 학습, 딥러닝 및 인공지능 기술의 발전으로 유방촬영 영상 판독의 과제를 해결하는 데 있어 영상의학과 전문의를 지원하는 것이 임상적으로 입증된 CAD 시스템의 개발이 가능해졌으며, 이는 암 검출률을 향상시키고 위양성 및 불필요한 환자 재검을 줄이는 동시에 판독 시간을 크게 단축시킨다.[^40]
자기공명영상(MRI)에 기반한 유방촬영술 평가 절차도 존재한다.
폐암 (기관지 암종)
폐암 진단에서는 특수한 3차원 CAD 시스템을 갖춘 컴퓨터 단층촬영이 확립되어 있으며 적절한 제2의견으로 간주된다.[^41] 이 과정에서 최대 3,000개의 개별 영상으로 구성된 용적 데이터셋이 준비되고 분석된다. 1 mm부터의 원형 병변(폐암, 전이 및 양성 변화)이 검출 가능하다. 현재 잘 알려진 모든 의료 시스템 공급업체가 해당 솔루션을 제공하고 있다.
폐암의 조기 발견은 매우 중요하다. 그러나 X선 영상에서 초기 단계(1기) 폐암을 우연히 발견하는 것은 어렵다. 5~10 mm 크기의 원형 병변은 쉽게 간과된다.[^42] CAD 흉부 시스템의 일상적 적용은 초기 의심 없이 작은 변화를 검출하는 데 도움이 될 수 있다. 다수의 연구자들이 흉부 방사선촬영[^43][^44][^45] 및 CT[^46][^47]에서의 폐결절(30 mm 미만의 원형 병변) 검출을 위한 CAD 시스템과 CT에서의 폐결절 진단(예, 악성과 양성의 구별)을 위한 CAD 시스템을 개발하였다. 가상 이중 에너지 영상[^48][^49][^50][^51]은 흉부 방사선촬영에서 CAD 시스템의 성능을 향상시켰다.
대장암
CAD는 CT 대장조영술에서 대장 내 대장 용종 검출에 사용 가능하다.[^5][^52] 용종은 대장 내벽에서 발생하는 작은 성장물이다. CAD는 용종의 특징적인 "돌출형" 형태를 식별하여 검출한다. 과도한 위양성을 방지하기 위해, CAD는 팽대주름을 포함한 정상 대장 벽을 무시한다.
심혈관 질환
심혈관 컴퓨팅, 심혈관 정보학, 수학적 및 계산적 모델링의 최신 방법은 임상 의사결정에 유용한 도구를 제공할 수 있다.[^53] 새로운 영상 분석 기반 표지자를 입력으로 사용하는 CAD 시스템은 혈관 전문의가 심혈관 질환 환자에게 가장 적합한 치료법을 더 높은 확신으로 결정하는 데 도움을 줄 수 있다.
경동맥 죽상동맥경화증의 신뢰할 수 있는 조기 발견 및 위험 계층화는 무증상 환자의 뇌졸중 예측에 매우 중요하다.[^54] 이를 위해 초음파 영상 기반 특징을 사용하는 다양한 비침습적이고 저비용의 표지자가 제안되었다.[^55] 이들은 에코발생도, 질감, 운동[^56][^57][^58][^59] 특성을 결합하여 심혈관 위험의 개선된 예측, 평가 및 관리를 위한 임상 의사결정을 지원한다.[^60]
CAD는 관상동맥 CT 혈관조영술(CCTA) 연구에서 유의미한(50% 이상의 협착을 유발하는) 관상동맥 질환의 자동 검출에 사용 가능하다.[^61]
선천성 심장 결함
병리의 조기 발견은 삶과 죽음의 차이를 만들 수 있다. CADe는 디지털 청진기와 전문 소프트웨어를 사용한 청진, 즉 컴퓨터 보조 청진을 통해 수행될 수 있다. 결함이 있는 심장을 통과하는 혈류에 의해 발생하는 비정상적 심장음인 심잡음은 높은 민감도와 특이도로 검출될 수 있다. 컴퓨터 보조 청진은 외부 소음과 신체음에 민감하며 정확하게 기능하기 위해 거의 무음의 환경을 필요로 한다.
병리학적 뇌 검출 (PBD)
Chaplot 등은 병리학적 뇌를 검출하기 위해 이산 웨이블릿 변환(DWT) 계수를 최초로 사용하였다.[^62] Maitra와 Chatterjee는 DWT의 개선된 버전인 슬랜틀릿 변환을 사용하였다. 각 영상의 특징 벡터는 특정 논리에 따라 선택된 여섯 개의 공간적 위치에 해당하는 슬랜틀릿 변환 출력의 크기를 고려하여 생성된다.[^63]
2010년, Wang과 Wu는 주어진 MR 뇌 영상을 정상 또는 비정상으로 분류하기 위한 순방향 신경망(FNN) 기반 방법을 제시하였다. FNN의 매개변수는 적응적 혼돈 입자 군집 최적화(ACPSO)를 통해 최적화되었다. 160개 영상에 대한 결과는 분류 정확도가 98.75%임을 보여주었다.[^64]
2011년, Wu와 Wang은 특징 추출에 DWT를, 특징 축소에 PCA를, 그리고 분류기로 스케일링된 혼돈 인공 벌 군집(SCABC)을 적용한 FNN을 사용할 것을 제안하였다.[^65]
2013년, Saritha 등은 병리학적 뇌를 검출하기 위해 웨이블릿 엔트로피(WE)를 최초로 적용하였다. Saritha는 또한 거미줄 도표의 사용을 제안하였다.[^6] 이후, Zhang 등은 거미줄 도표를 제거해도 성능에 영향을 미치지 않음을 증명하였다.[^66] 정상 대조군에서 비정상 뇌를 식별하기 위해 유전자 패턴 탐색 방법이 적용되었다. 분류 정확도는 95.188%로 보고되었다.[^67] Das 등은 리플릿 변환의 사용을 제안하였다.[^68] Zhang 등은 입자 군집 최적화(PSO)의 사용을 제안하였다.[^69] Kalbkhani 등은 GARCH 모델의 사용을 제안하였다.[^70]
2014년, El-Dahshan 등은 펄스 결합 신경망의 사용을 제안하였다.[^71]
2015년, Zhou 등은 병리학적 뇌를 검출하기 위한 나이브 베이즈 분류기의 적용을 제안하였다.[^72]
알츠하이머병
CAD는 정상 노인 대조군에서 알츠하이머병 및 경도인지장애 피험자를 식별하는 데 사용될 수 있다.
2014년, Padma 등은 AD 양성 및 악성 종양 절편을 분할하고 분류하기 위해 결합된 웨이블릿 통계적 질감 특징을 사용하였다.[^6] Zhang 등은 커널 서포트 벡터 머신 결정 트리가 80%의 분류 정확도를 가지며, 각 영상 분류에 대한 평균 계산 시간이 0.022초임을 발견하였다.[^73]
2019년, Signaevsky 등은 알츠하이머병 및 다양한 타우병증에서 신경원섬유 매듭(NFT)의 검출 및 정량화를 위해 훈련된 완전 합성곱 네트워크(FCN)를 최초로 보고하였다. 훈련된 FCN은 200 에포크 동안 훈련된 SegNet 모델을 사용하여 NFT 객체를 올바르게 식별하는 미경험 디지털 전체 슬라이드 영상(WSI) 의미론적 분할에서 높은 정밀도와 재현율을 달성하였다. FCN은 그래픽 처리 장치(GPU)당 WSI 하나에 평균 45분의 처리 시간으로 거의 실용적 수준의 효율성에 도달하여 NFT의 신뢰할 수 있고 재현 가능한 대규모 검출을 가능하게 하였다. 다양한 타우병증에 걸친 8개의 미경험 WSI로 구성된 테스트 데이터에서 측정된 성능은 재현율, 정밀도, F1 점수가 각각 0.92, 0.72, 0.81이었다.[^74]
고유뇌(Eigenbrain)는 주성분 분석(PCA)[^75] 또는 독립 성분 분석 분해[^76]에 기반하여 AD 검출에 도움을 줄 수 있는 새로운 뇌 특징이다. 다항 커널 SVM이 우수한 정확도를 달성하는 것으로 나타났다. 다항 KSVM은 선형 SVM 및 RBF 커널 SVM보다 더 나은 성능을 보인다.[^77] 양호한 결과를 보이는 다른 접근법으로는 질감 분석,[^78] 형태학적 특징,[^79] 또는 고차 통계적 특징[^80]의 사용이 있다.
핵의학
CADx는 핵의학 영상에 사용 가능하다. 전신 골 스캔에서의 골전이 진단 및 심근 관류 영상에서의 관상동맥 질환 진단을 위한 상용 CADx 시스템이 존재한다.[^81]
높은 민감도와 허용 가능한 위양성 병변 검출률로, 컴퓨터 보조 자동 병변 검출 시스템은 유용한 것으로 입증되었으며 향후 핵의학 전문의가 가능한 골 병변을 식별하는 데 도움을 줄 수 있을 것으로 예상된다.[^82]
당뇨병성 망막병증
당뇨병성 망막병증은 주로 안저 영상으로 진단되는 망막 질환이다. 선진국의 당뇨병 환자들은 일반적으로 이 질환에 대한 정기적인 선별검사를 받는다. 영상은 비정상적인 망막 혈관의 초기 징후를 인식하는 데 사용된다. 이러한 영상의 수동 분석은 시간이 많이 소요되고 신뢰할 수 없을 수 있다.[^7][^8] CAD는 자동 검출 방법의 정확도, 민감도 및 특이도를 향상시키기 위해 사용되어 왔다. 일부 CAD 시스템을 인간 판독자 대신 사용하는 것은 안전하고 비용 효과적일 수 있다.[^8]
영상 전처리, 특징 추출 및 분류는 이러한 CAD 알고리즘의 두 가지 주요 단계이다.[^9]
전처리 방법
영상 정규화는 전체 영상에 걸친 변동을 최소화하는 것이다. 눈의 주변부와 중심 황반 영역 사이의 강도 변동이 혈관 분할의 부정확성을 유발하는 것으로 보고되었다.[^83] 2014년 리뷰에 따르면, 이 기법은 가장 자주 사용되었으며 최근(2011년 이후) 발표된 40개의 원저 연구 중 11개에 등장하였다.[^9]
![히스토그램 평활화 예시 영상. 왼쪽: 일반 회색조 안저 영상. 오른쪽: 히스토그램 평활화 처리 후.^84 ] 히스토그램 평활화는 영상 내 대비를 향상시키는 데 유용하다.[^85] 이 기법은 국소 대비를 증가시키는 데 사용된다. 처리가 끝나면, 입력 영상에서 어두웠던 영역이 밝아져 해당 영역에 존재하는 특징들 간의 대비가 크게 향상된다. 반면, 입력 영상에서 밝았던 영역은 밝기가 유지되거나 영상의 다른 영역과 균등화되도록 밝기가 감소된다. 혈관 분할 외에도, 당뇨병성 망막병증과 관련된 다른 특징들도 이 전처리 기법을 사용하여 추가로 분리할 수 있다. 미세동맥류와 출혈은 적색 병변이며, 삼출물은 황색 반점이다. 이 두 그룹 간의 대비를 증가시키면 영상에서 병변의 시각화가 향상된다. 이 기법에 대해 2014년 리뷰에서는 최근(2011년 이후) 발표된 14개의 원저 연구 중 10개에서 확인되었다.[^9]
녹색 채널 필터링은 혈관보다는 병변을 구별하는 데 유용한 또 다른 기법이다. 이 방법은 당뇨병성 망막병증 관련 병변 간의 최대 대비를 제공하기 때문에 중요하다.[^86] 미세동맥류와 출혈은 녹색 채널 필터링 적용 후 어둡게 나타나는 적색 병변이다. 반면, 정상 영상에서 황색으로 나타나는 삼출물은 녹색 필터링 후 밝은 흰색 반점으로 변환된다. 2014년 리뷰에 따르면 이 기법이 가장 많이 사용되었으며, 지난 3년간 발표된 40개 논문 중 27개에 등장하였다.[^9] 또한, 녹색 채널 필터링은 이중 창 시스템과 결합하여 시신경유두의 중심을 검출하는 데 사용될 수 있다.
비균일 조명 보정은 안저 영상의 비균일 조명을 조정하는 기법이다. 비균일 조명은 영상의 통계적 특성 변화로 인해 당뇨병성 망막병증의 자동 검출에서 잠재적 오류가 될 수 있다.[^9] 이러한 변화는 특징 추출과 같은 후속 처리에 영향을 미칠 수 있으며 인간에 의해 관찰되지 않는다. 비균일 조명 보정(f')은 알려진 원래 픽셀 강도(f), 국소(λ) 및 원하는 픽셀(μ)의 평균 강도를 사용하여 픽셀 강도를 수정함으로써 달성할 수 있다(아래 수식 참조).[^10] 그런 다음 Walter-Klein 변환을 적용하여 균일한 조명을 달성한다.[^10] 이 기법은 2014년 리뷰에서 가장 적게 사용된 전처리 방법이다.
f' = f + \mu-\lambda
형태학적 연산은 2014년 리뷰에서 두 번째로 적게 사용된 전처리 방법이다.[^9] 이 방법의 주요 목적은 특히 배경 대비 어두운 영역의 대비 향상을 제공하는 것이다.
특징 추출 및 분류
안저 영상의 전처리 후, 영상은 다양한 계산적 방법을 사용하여 추가 분석된다. 그러나 현재 문헌에서는 혈관 분할 분석 시 일부 방법이 다른 것보다 더 자주 사용된다는 데 동의하고 있다. 이러한 방법에는 SVM, 다중 스케일, 혈관 추적, 영역 성장 접근법 및 모델 기반 접근법이 있다.
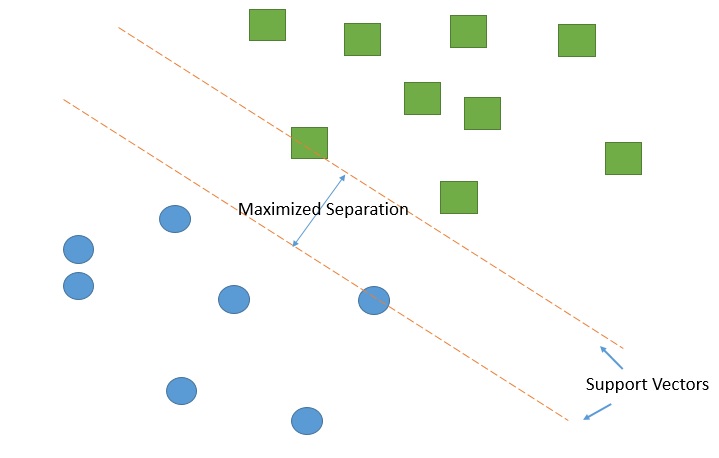
서포트 벡터 머신은 혈관 분할에서 가장 자주 사용되는 분류기로, 최대 90%의 사례에서 사용된다. SVM은 패턴 인식 기법의 더 넓은 범주에 속하는 지도 학습 모델이다. 이 알고리즘은 데이터에서 서로 다른 샘플 간의 가장 큰 간격을 생성하여 작동한다. 목표는 분류 오류를 최소화하는 이러한 구성 요소 간의 가장 큰 간격을 만드는 것이다.[^11] 눈 영상의 나머지 부분에서 혈관 정보를 성공적으로 분리하기 위해, SVM 알고리즘은 지도 환경을 통해 혈관 픽셀을 영상의 나머지 부분과 분리하는 서포트 벡터를 생성한다. 새로운 영상에서의 혈관 검출은 서포트 벡터를 사용하여 유사한 방식으로 수행될 수 있다. 녹색 채널 필터링과 같은 다른 전처리 기법과의 조합은 혈관 이상 검출의 정확도를 크게 향상시킨다.[^9] SVM의 일부 유용한 특성은 다음과 같다.[^11]
- 유연성 – 기능 면에서 매우 유연함
- 단순성 – 특히 대규모 데이터셋에서 단순함(데이터 간 분리를 생성하는 데 서포트 벡터만 필요) 다중 스케일 접근법은 혈관 분할에서의 다중 해상도 접근법이다. 낮은 해상도에서는 큰 직경의 혈관이 먼저 추출될 수 있다. 해상도를 높이면 큰 혈관에서 나오는 작은 분지가 쉽게 인식될 수 있다. 따라서 이 기법을 사용하는 한 가지 장점은 분석 속도의 향상이다.[^7] 또한, 이 접근법은 3D 영상에 사용될 수 있다. 표면 표현은 혈관의 곡률에 수직인 표면으로, 혈관 표면의 이상을 검출할 수 있게 한다.
혈관 추적은 혈관의 "중심선"을 검출하는 알고리즘의 능력이다. 이 중심선은 혈관 곡률의 최대 봉우리이다. 혈관의 중심은 가우시안 필터에 의해 제공되는 방향 정보를 사용하여 찾을 수 있다. 중심선 개념을 활용하는 유사한 접근법에는 골격 기반 및 미분 기하학 기반이 있다.[^7]
영역 성장 접근법은 유사성을 가진 이웃 픽셀을 검출하는 방법이다. 이러한 방법이 시작되려면 시드 포인트가 필요하다. 이 기법이 작동하려면 두 가지 요소가 필요하다: 유사성과 공간적 근접성. 유사한 강도를 가진 시드 픽셀의 이웃 픽셀은 같은 유형일 가능성이 높으며 성장하는 영역에 추가된다. 이 기법의 한 가지 단점은 시드 포인트의 수동 선택이 필요하여 알고리즘에 편향과 불일치를 도입한다는 것이다.[^7] 이 기법은 시신경유두 식별에도 사용되고 있다.
모델 기반 접근법은 영상에서 혈관을 추출하기 위해 표현을 사용한다. 모델 기반의 세 가지 큰 범주는 변형 가능, 매개변수적, 템플릿 매칭으로 알려져 있다.[^7] 변형 가능 방법은 영상의 객체 윤곽에 맞도록 변형될 객체를 사용한다. 매개변수적 방법은 혈관의 관형, 원통형 또는 타원체 표현과 같은 기하학적 매개변수를 사용한다. 고전적 스네이크 윤곽과 혈관 위상 정보의 조합도 모델 기반 접근법으로 사용될 수 있다.[^87] 마지막으로, 템플릿 매칭은 은닉 마르코프 모델 1을 사용한 확률적 변형 과정에 의해 적합된 템플릿의 사용이다.
고용에 대한 영향
의료 진단 노동의 자동화(예: 적혈구 정량화)는 일정한 역사적 선례가 있다.[^88] 2010년대의 딥러닝 혁명은 이미 영상의학과 전문의와 피부과 전문의보다 많은 시각적 진단 영역에서 더 정확한 AI를 만들어냈으며, 이 격차는 더욱 벌어질 것으로 예상된다.
많은 의사를 포함한 일부 전문가들은 AI가 의료 전문 분야에 미칠 영향을 대수롭지 않게 여긴다.
이와 대조적으로, 많은 경제학자와 인공지능 전문가들은 영상의학과 같은 분야가 대규모로 변혁을 겪을 것이며, 영상의학과 전문의의 실업이나 임금 하락 압력이 발생할 것이라고 믿는다. 병원은 전반적으로 더 적은 수의 영상의학과 전문의를 필요로 할 것이며, 여전히 남아 있는 영상의학과 전문의 중 다수는 상당한 재교육이 필요할 것이다. "딥러닝의 대부"로 불리는 제프리 힌턴은 향후 5년에서 10년 내에 예상되는 발전을 고려할 때, 병원은 즉시 영상의학과 전문의 양성을 중단해야 한다고 주장한다. 시각적 진단에 대한 시간과 비용이 많이 드는 교육이 곧 대부분 구식이 되어 전통적인 영상의학과 전문의의 공급 과잉으로 이어질 것이기 때문이다.[^89][^90]
JAMA에 실린 한 논평은 병리학자와 영상의학과 전문의가 단일한 "정보 전문가" 역할로 통합되어야 한다고 주장하며, "컴퓨터에 의해 대체되는 것을 피하려면, 영상의학과 전문의는 스스로 컴퓨터에 의해 대체되는 것을 허용해야 한다"고 밝히고 있다. 정보 전문가는 "베이즈 논리, 통계학, 데이터 과학"과 일부 유전체학 및 생체인식학에 대한 교육을 받게 되며, 수동적인 시각적 패턴 인식은 현재의 부담스러운 영상의학 수련과 비교하여 크게 비중이 줄어들 것이다.[^91]
같이 보기
- 임상시험에 사용되는 컴퓨터 시스템
- 마이신
- 로봇 수술
각주
외부 링크
- Digital Retinal Images for Vessel Extraction (DRIVE)
- STructured Analysis of the REtina (STARE)
- 고해상도 안저(HRF) 이미지 데이터베이스
참고 문헌
[^1]: cite journal vauthors = Yanase J, Triantaphyllou E title = 의학에서의 컴퓨터 보조 진단에 대한 체계적 조사: 과거와 현재의 발전. journal = Expert Systems with Applications
[^2]: citation author1=Salcudean, S. E. author2=Bell, G. author3=Bachmann, S. author4=Zhu, W. H. author5=Abolmaesumi, P. author6=Lawrence, P. D. title = 로봇 보조 진단 초음파 - 설계
[^3]: citation author1=Dario, P. author2=Bergamasco, M. year = 1988 title = 촉진을 통한 자동 진단 작업을 위한 고급 로봇 시스템 journal = IEEE Transactions on Biomedical Engineeri
[^4]: cite journal vauthors = Yanase J, Triantaphyllou E title = 의학에서의 컴퓨터 보조 진단의 미래를 위한 7가지 핵심 과제. journal = International Journal of Medical Informatics
[^5]: Cite journal doi=10.1016/j.crad.2018.02.009 pmid=29602538 title = 대장 용종 식별을 위한 컴퓨터 보조 검출(CAD) 프로그램 비교: 성능 및 민감도
[^6]: Cite journal doi=10.1007/s13369-013-0649-3 title = 결합 웨이블릿 통계 텍스처 특징을 이용한 뇌 CT 영상의 분할 및 분류 journal=[[Arabian Journal for Science and E
[^7]: Kaur, M. 혈관 추출 및 눈 망막병증 검출에 대한 리뷰
[^8]: Tufail, A. 자동 당뇨망막병증 영상 평가 소프트웨어: 인간 판독자와 비교한 진단 정확도 및 비용 효율성. (n.d.)
[^9]: Ahmad, A.. 2014 제5회 유럽 시각 정보 처리 워크숍 (EUVIP). (2014-12-01)
[^10]: Antal, B.. 미세동맥류 검출 및 당뇨망막병증 등급화를 위한 앙상블 기반 시스템. (2012-06-01)
[^11]: Administrator. SVM과 MDA를 이용한 당뇨망막병증 검출에 대한 리뷰. (2015-05-20)
[^12]: 컴퓨터 보조 진단: 디지털 병리학의 전환점. Digital Pathology Association. (27 April 2017)
[^13]: Oakden-Rayner, Luke. CAD의 부활: 현대 AI는 우리가 알고 있는 CAD와 어떻게 다른가?. (May 2019)
[^14]: Bird, R. E.. 선별 유방촬영술에서 놓친 암의 분석. (1992)
[^15]: Baker, J. A.. 선별 유방촬영술에서의 컴퓨터 보조 검출(CAD): 구조적 왜곡 검출을 위한 상용 CAD 시스템의 민감도. (2003)
[^16]: Jang, H. J.. 세기관지폐포암: 박절 CT에서 간유리 감쇠의 국소 영역이 초기 징후로서. (1996)
[^17]: Suzuki, K.. 대규모 훈련 인공 신경망을 이용한 흉부 저선량 CT에서 양성 및 악성 결절 구별을 위한 컴퓨터 보조 진단 체계. (2005)
[^18]: Lostumbo, A.. CT 대장조영술에서의 편평 병변. (2010)
[^19]: Lea, Andrew S.. 진단의 디지털화: 20세기 미국의 의학, 정신, 그리고 기계. Johns Hopkins University Press
[^20]: cite journal vauthors = Shortliffe EH, and Buchanan BG title = 의학에서의 부정확한 추론 모델. journal = Mathematical Biosciences date = 1975 volume = 23 issue = 3–4 pages = 351–3
[^21]: cite journal vauthors = Miller RA, Pople Jr HE, and Myers JD title = Internist-I, 일반 내과를 위한 실험적 컴퓨터 기반 진단 자문 시스템. journal = New England Journa
[^22]: Feigenbaum, Edward. 제5세대. Addison-Wesley
[^23]: cite book author = Richard M. Karp chapter = 조합 문제들 간의 환원 가능성 chapter-url = http://www.cs.berkeley.edu/~luca/cs172/karp.pdf title = Complexity of Computer Computations
[^24]: cite journal vauthors = Doi K title = 의료 영상에서의 컴퓨터 보조 진단: 역사적 검토, 현재 상태 및 미래 잠재력. journal = Computerized Medical Imaging and Graphics d
[^25]: Upbin, Bruce. IBM의 왓슨, 헬스케어 분야에서 첫 사업을 확보하다. (2013-02-08)
[^27]: Echegaray, Sebastian. 종양 분할에 둔감한 방사선체학 특징을 위한 코어 샘플: 간세포암 CT 영상을 이용한 방법 및 예비 연구. (18 November 2015)
[^28]: Murphy, K.. 국소 영상 특징 및 k-최근접 이웃 분류를 이용한 흉부 CT에서의 자동 폐 결절 검출에 대한 대규모 평가. (2009)
[^29]: Suzuki, K.. 저선량 컴퓨터 단층촬영에서의 폐 결절 전산 검출 시 위양성 감소를 위한 대규모 훈련 인공 신경망(MTANN). (2003)
[^30]: Chan, H. P.. 유방촬영 미세석회화의 컴퓨터 보조 검출: 인공 신경망을 이용한 패턴 인식. (1995)
[^31]: Gletsos, Miltiades. CT 국소 간 병변 특성화를 위한 컴퓨터 보조 진단 시스템: 신경망 분류기의 설계 및 최적화. (2003)
[^32]: Mougiakakou, Stavroula. 초음파 영상 통계, Laws 텍스처 및 신경망을 기반으로 한 경동맥 죽상경화증의 컴퓨터 보조 진단. (2007)
[^33]: Stoitsis, John. 의료 영상 처리 및 인공 지능 방법에 기반한 컴퓨터 보조 진단. (2006)
[^34]: Chen, S.. 서포트 벡터 분류를 이용한 2단계 결절 강화에 의한 흉부 방사선 사진에서의 폐 결절 검출을 위한 컴퓨터 보조 진단 체계의 개발 및 평가. (2011)
[^35]: Papadopoulos, A.. 신경망 및 서포트 벡터 머신을 이용한 디지털 유방촬영에서의 군집 미세석회화 특성화. (2005)
[^36]: cite journal author1=Wollenweber T. author2=Janke B. author3=Teichmann A. author4=Freund M. year = 2007 title = 조직학적 소견과 컴퓨터 보조 검출 간의 상관관계 journal = Progress in Elec
[^37]: 동시 유전 질환 식별을 위한 컴퓨터 기반 진단 도구의 정확도
[^38]: cite journal vauthors = Bron EE, Smits M, Van Der Flier WM, Vrenken H, Barkhof F, Scheltens P, Papma JM, Steketee RM, Orellana CM, Meijboom R, and Pinto M title = 알고리즘의 표준화된 평가
[^39]: cite journal vauthors=Taylor P, Potts HW year = 2008 title = 선별 유방촬영술에서의 개입으로서의 컴퓨터 보조 및 인간 이중 판독: 암에 대한 효과를 비교하기 위한 두 가지 체계적 검토
[^40]: Benjamens, Stan. 인공지능 기반 FDA 승인 의료기기 및 알고리즘의 현황: 온라인 데이터베이스. (2020)
[^41]: Abe, Yoshiyuki. 컴퓨터 단층촬영을 이용한 폐암 선별검사에서의 컴퓨터 보조 진단(CAD) 시스템. (2005-01-01)
[^42]: cite journal vauthors=Wu N, Gamsu G, Czum J, Held B, Thakur R, Nicola G date = Mar 2006 title = 직접 디지털 방사선촬영 및 영상 저장 전송 시스템을 이용한 소폐 결절 검출 com
[^43]: Giger, Maryellen Lissak. 디지털 방사선촬영에서의 영상 특징 분석 및 컴퓨터 보조 진단. 3. 말초 폐야에서의 결절 자동 검출. (1988-03-01)
[^44]: Ginneken, B. Van. 흉부 방사선촬영에서의 컴퓨터 보조 진단: 조사. (2001-12-01)
[^45]: Coppini, G.. 컴퓨터 보조 진단을 위한 신경망: 흉부 방사선 사진에서의 폐 결절 검출. (2003-12-01)
[^46]: Giger, M. L.. 컴퓨터 단층촬영 영상에서의 폐 결절 전산 검출. (1994-04-01)
[^47]: Kanazawa, K.. 나선형 CT 영상을 기반으로 한 폐 결절의 컴퓨터 보조 진단. (1998-03-01)
[^48]: Chen, Sheng. 뼈 억제 및 일관된 처리를 통한 중환자실에서 촬영된 흉부 방사선 사진의 향상
[^49]: Chen, S.. 해부학적 특화 다중 대규모 훈련 ANN과 전체 변분 최소화 평활화를 결합한 흉부 방사선 사진에서의 뼈 분리. (2014-02-01)
[^50]: Suzuki, K.. 대규모 훈련 인공 신경망(MTANN)을 이용한 흉부 방사선 사진에서의 늑골 억제를 위한 영상 처리 기술. (2006-04-01)
[^51]: LOOG, M. 필터 학습: 흉부 방사선 사진에서 뼈 구조 억제에의 적용. (2006-12-01)
[^52]: Suzuki, Kenji. 컴퓨터 보조 용종 검출에서 위양성 감소를 위한 대규모 훈련 인공 신경망(MTANN): 직장관 억제. (2006-10-01)
[^53]: Golemati, Spyretta. 심혈관 컴퓨팅 - 방법론 및 임상 응용. Springer. (2019)
[^54]: Gastounioti, Aimilia. 동맥벽의 운동학적 특징을 이용한 경동맥 죽상경화증의 위험 계층화를 위한 새로운 전산 도구. (2014)
[^55]: Golemati, Spyretta. 무증상 경동맥 죽상경화증에서 뇌졸중 예측을 위한 새로운 비침습적 저비용 표지자를 향하여: 초음파 영상 분석의 역할. (2013)
[^56]: Golemati, Spyretta. B-모드 초음파에서 경동맥 죽상경화반의 운동 동기화 패턴. (2020)
[^57]: Rizi, Fereshteh. 초음파 영상에서의 경동맥 벽 종방향 운동: 전문가 합의 검토. (2020)
[^58]: Golemati, Spyretta. 초음파 영상 기반 심혈관 조직 운동 추정. (2016)
[^59]: Gastounioti, Aimilia. 적응적 블록 매칭을 이용한 B-모드 초음파에서의 경동맥 벽 운동 분석: 시뮬레이션 평가 및 생체 내 적용. (2013)
[^60]: Gastounioti, Aimilia. CAROTID - 죽상경화 환자의 최적 개인맞춤 관리를 위한 웹 기반 플랫폼. (2014)
[^61]: Goldenberg, Roman. 관상동맥 CT 혈관조영술(CCTA)을 위한 컴퓨터 보조 단순 분류(CAST). (2012)
[^62]: cite journal doi=10.1016/j.bspc.2006.05.002 title=서포트 벡터 머신 및 신경망의 입력으로 웨이블릿을 사용한 자기공명 뇌 영상 분류 year=2006 last1=Chaplot
[^63]: cite journal doi=10.1016/j.bspc.2006.12.001 title=슬랜틀릿 변환 기반 자기공명 뇌 영상 분류를 위한 지능형 시스템 year=2006 last1=Maitra first1=Madhubanti l
[^64]: Wang, S.. 적응적 혼돈 PSO를 기반으로 한 자기공명 뇌 영상 분류의 새로운 방법. (2010)
[^65]: Zhang, Yudong. 개선된 인공 벌 군집 알고리즘에 의한 자기공명 뇌 영상 분류. (2011)
[^66]: Zhang, Yudong. MR 뇌 영상 분류에서 거미줄 도표의 효과. (2015)
[^67]: Zhang, Y.. 유전 패턴 탐색 및 뇌 영상 분류에의 적용. (2013)
[^68]: cite journal author1=Das S. author2=Chowdhury M. author3=Kundu M.K. year = 2013 title = 리플릿의 다중 스케일 기하학적 분석을 이용한 뇌 MR 영상 분류 journal = Progress in Elec
[^69]: Zhang, Y.. 입자 군집 최적화 및 커널 서포트 벡터 머신을 통한 MR 뇌 영상 분류 시스템. (2013)
[^70]: cite journal author1=Kalbkhani H. author2=Shayesteh M.G. author3=Zali-Vargahan B. year = 2013 title = GARCH 분산 모델을 기반으로 한 뇌 자기공명영상(MRI) 분류를 위한 강건한 알고리즘
[^71]: cite journal author1=El-Dahshan E.S.A. author2=Mohsen H.M. author3=Revett K. year = 2014 title = MRI를 통한 인간 뇌종양의 컴퓨터 보조 진단: 조사 및 새로운 알고리즘 journa
[^72]: Zhou, Xing-Xing. 생물정보학 및 생의학 공학. (2015)
[^73]: Zhang, Yudong. 커널 서포트 벡터 머신 결정 트리에 의한 구조적 자기공명영상 기반 알츠하이머병 분류. (2014)
[^74]: Signaevsky, Maxim. 신경병리학에서의 인공지능: 타우병증의 딥러닝 기반 평가
[^75]: Friston, K.. PET 활성화 연구의 다변량 분석. (1996)
[^76]: Martínez-Murcia, F.J.. 유의성 측정 및 독립 성분 분석에 기반한 기능적 활동 지도. (2013)
[^77]: Dong, Z.C.. 고유뇌 및 기계 학습을 기반으로 한 3D MRI 스캔을 이용한 알츠하이머병 관련 대상자 및 뇌 영역 검출. (2015)
[^78]: Zhang, J.. 알츠하이머병의 MRI 영상에 대한 3D 텍스처 분석. (2012)
[^79]: Chupin, Marie. ADNI 데이터에 적용된 알츠하이머병 및 경도 인지 장애에서의 완전 자동 해마 분할 및 분류. (2009)
[^80]: Martinez-Murcia, F.J.. 알츠하이머병 검출을 위한 MR 영상의 구면 뇌 매핑.. (2016)
[^81]: EXINI Diagnostics
[^82]: Huang, Kao and Chen. 핵의학 전신 골 스캔 영상에서의 컴퓨터 보조 진단을 위한 영상 처리 알고리즘 세트. (18 June 2007)
[^83]: Fraz, M. M.. 비트 평면 및 중심선 검출을 이용한 망막 혈관 위치 파악 방법. (2012-11-01)
[^84]: Priya, R. 서포트 벡터 머신을 이용한 당뇨망막병증 자동 진단에 대한 리뷰
[^85]: Abedin, Zain ul. CAD/CAM이란 무엇인가?. (2023-11-10)
[^86]: Saleh, Marwan D.. 미세동맥류 및 출혈 검출에 기반한 비증식성 당뇨망막병증 질환을 위한 자동 의사결정 지원 시스템. (2012-10-01)
[^87]: Espona, L.. 패턴 인식 및 영상 분석. Springer Berlin Heidelberg. (2007-06-06)
[^88]: Paiva, Omir Antunes. 방사선학에서 인공지능의 잠재적 영향. (October 2017)
[^89]: Mukherjee, Siddhartha. 인공지능 대 의사. (27 March 2017)
[^90]: 스캔 판독 인공지능이 영상의학과 의사에게 나쁜 소식인 이유. (29 November 2017)
[^91]: Jha, Saurabh. 인공지능에의 적응. (13 December 2016)
관련 인사이트

공장의 뇌는 어떻게 생겼는가 — 제조운영 AI 아키텍처 해부
지식관리, 업무자동화, 의사결정지원 — 따로 보면 다 있던 것들입니다. 제조 AI의 진짜 차이는 이 셋이 순환하면서 '우리 공장만의 지능'을 만든다는 데 있습니다.

그 30분을 18년 동안 매일 반복했습니다 — 품질팀장이 본 AI Agent
18년차 품질팀장이 매일 아침 30분씩 반복하던 데이터 분석을 AI Agent가 3분 만에 해냈습니다. 챗봇과는 완전히 다른 물건 — 직접 시스템에 접근해서 데이터를 꺼내고 분석하는 AI의 현장 도입기.
ERP 20년, 나는 왜 AI를 얹기로 했나
ERP 20년차 제조IT본부장의 고백: 3,200만 행의 데이터가 잠들어 있었다. ERP를 바꾸지 않고 AI를 얹자, 일주일 걸리던 불량 분석이 수 초로 줄었다.